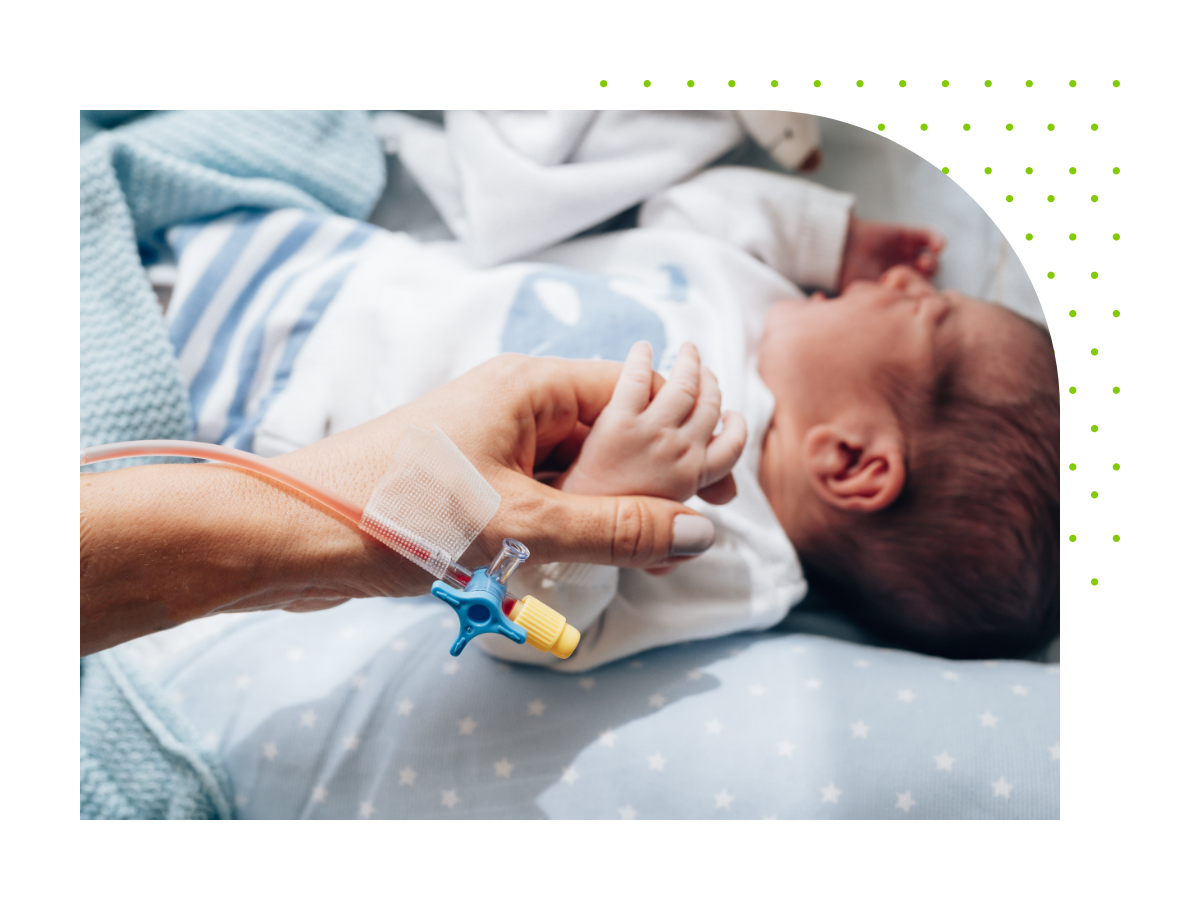
医疗器械质量管理与合规软件解决方案
我们的法规事务管理平台(RAMS)依托数十年的法规合规经验,可作为您的软件即服务(SaaS)解决方案,辅助传统的 RA/QA(法规事务/质量管理)咨询服务。您将能够接触由医疗器械和体外诊断器械(IVD)RA/QA 专家、行业专业人员组成的资源网络,同时利用其所提供的欧盟代表服务,以及专业的质量管理体系(QMS)和培训服务。
RAMS 深受 15000 多家医疗器械公司的信赖





简化欧盟医疗器械法规合规工作
由 Emergo by UL 的专家开发的 RAMS 提供不断扩展的欧盟 MDD、MDR 和 IVDR 服务组合,其中包括 Product Classification 和七个 Smart Builder,为计划向欧盟新法规过渡的企业提供重要支持。
RAMS 在医疗器械合规管理方面的成果



通过智能软件管理合规事务
体验三个墨西哥等同路径和标准路径 Smart Builder 和 IVDR Regulatory Essentials 报告,以及一款免费的 Global Fee Finder 工具。

助力获得医疗器械的市场准入

简化医疗器械产品分类工作
利用 Product Classification 简化市场准入的第一步。通过一系列简明的引导式问题,您可在几分钟内确定器械分类或验证现有分类,助力节省时间,自信地开始构建上市路线图。


从容应对各市场的医疗器械法规
通过 Regulatory Reports 缩短上市所需时间并降低成本。利用按国家/地区、器械类型和器械类别分类的监管分析信息,探索新市场。借助针对各市场的详细指南,在审批后持续保持市场合规,有助于减少代价高昂的业务中断。

在医疗器械市场助推成长

智能合规软件
Regulatory Intelligence 依托整合了全球知识库的流程图和常见问题解答,协助您洞察目标市场的要求,战略性地规划后续行动以申请获得其他国家/地区的市场准入。
RAMS 捆绑服务方案
强大功能助力您规划并拓展医疗器械或体外诊断器械(IVD)业务。
建立账户以进一步了解 RAMS 捆绑软件。
| Emergo Pro | Emergo Pro+ | |
|---|---|---|
Product Classification通过器械分类和验证服务,助力简化申请市场准入的第一步。 | ||
Regulatory Reports通过按国家/地区、器械类型和器械类别分类的监管分析信息,助力探索新市场。 | 3 个市场 | 不限数量的市场 |
Regulatory Watch追踪法规变化,即时洞察这些变化对医疗器械注册的影响。 | ||
Registration Tracker借助自动化的注册与认证追踪流程,简化合规工作,提醒证书更新事宜,节省时间。 | ||
Regulatory Intelligence通过整合了全球知识库的流程图和常见问题解答,助力规划业务扩张之旅。 | ||
授权用户数量 | 5 个用户 | 10 个用户 |
医疗器械质量管理解决方案
医疗器械质量管理软件
借助基于云的先进质量管理体系(QMS)软件 Greenlight Guru,助力效率提升。升级现有的纸质或通用质量管理体系,让您能够在云端跟踪质量事件、管理设计控制风险、验证合规性等。Greenlight Guru 针对医疗技术的独特挑战和严格要求进行了优化,通过单一信息源,高效对接相关人员、流程和数据。
面向医疗科技专业人员的优质培训
ComplianceWire 是一款基于网络的主流平台,专为受高度监管的行业而设计。这个学习管理系统(LMS)简化了合规培训计划的创建与自动化管理,自 1999 年以来,美国食品药品监督管理局便已使用该平台为 4 万多名调查员提供培训服务。该系统通过强大的基于角色的培训自动化功能,助力提高产品安全,记录人员资质信息。
向我们的专家们询问信息
感谢您对我们的产品和服务感兴趣。请允许我们收集一些信息,以便安排合适的工作人员与您联系。